2023 Therascience 年会 – 后生元
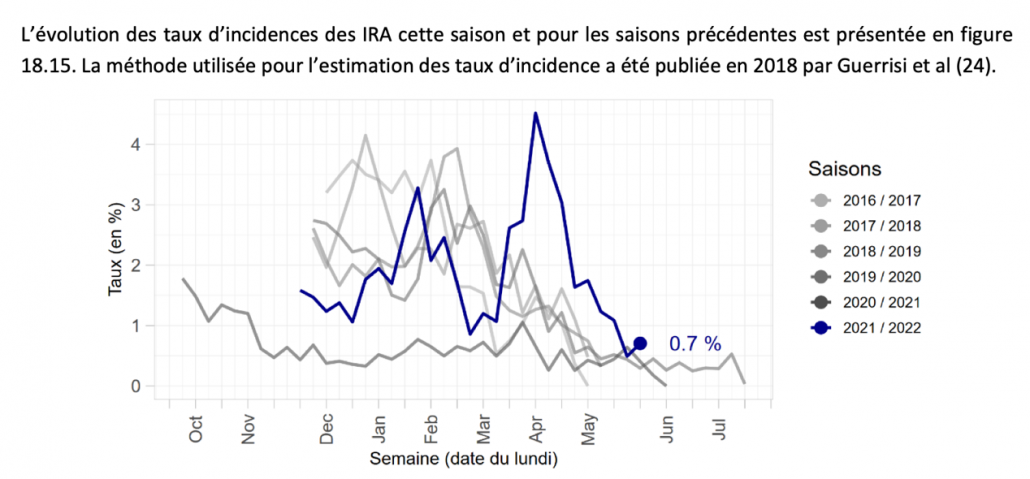
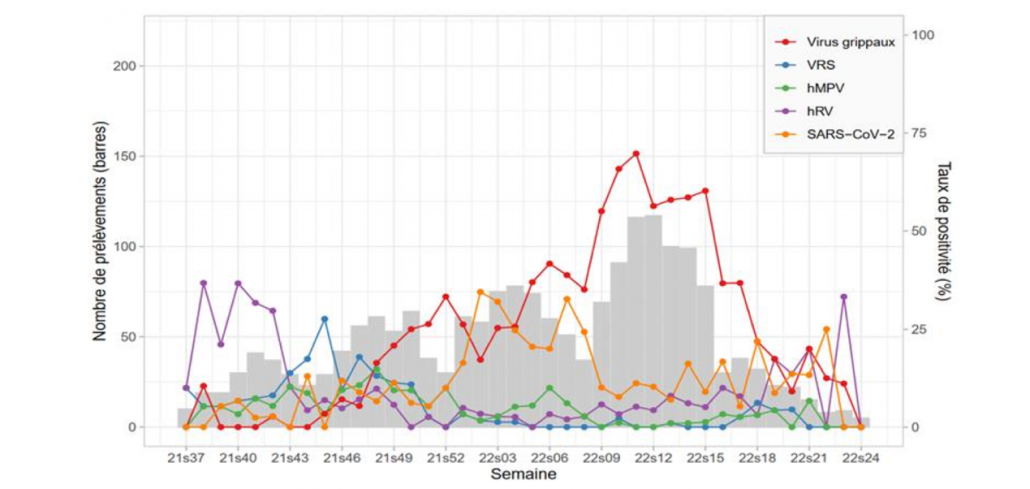
2023年Therascience年会由杰瑞姆, 米勒万诺夫(Jerome MILOVANOFF)医生分享了法国的急性呼吸道疾病的趋势。根据家庭医生数据显示,法国经历了两个比较明显的峰值。一是从2021年12月份到2022年2月份,这期间的急性呼吸道疾病主要和新冠有关。另外一个高峰期是甲感的爆发从3月份一直持续到4月底。
除了医生的治疗方案,米勒万诺夫医生认为营养素可以支持免疫系统以及帮助抵抗力。除了熟知的益生元,益生菌产品, 还有后生元产品。
后生元是益生菌经加工处理后的益生菌代谢物成分统称,包括菌体与代谢产物。研究证实,经过筛选的后生元,增强免疫能力优于原活菌,即使经由高温作用或肠胃消化液处理,仍保有高度生理活性 【1】。后生元的代表成分 (例如: 脂壁酸) 是决定后生元对于酸、碱、热耐受性的关键 【2】【4】。
新的科研指出,益生菌对身体健康有益帮助不一定和活菌有直接关系,可能是活菌的代谢产物或菌体成分才是促进健康的推手 【3】 。因此,科学家渐渐注意到益生菌具有健康的功能是建立在他们的菌体本身、代谢物、或是裂解产物,这些因子正式被国际益生菌组织命名为“后生元”【1】【3】。后生元和活菌自然死亡 (死菌) 对健康的效应是完全不同,关键在于“是否能保存活效因子?”。唯有经特殊处理 (例如: 热灭活) 的后生元,保存其特殊的活效因子 ,而此特性将开启益生菌产业对于益生菌产品的新应用和革新。
德诺海科实验室Teoliance系列新推出的后生元Postbiot,在第一代产品丁酸盐的基础上,含有2种生物活性物质的协同作用,由蛋白质、纤维、多酚、维生素、氨基酸和多糖(β-葡聚糖和甘露聚糖)组成,具有多成分活性成分的额外优势,这是单一生物活性成分难以实现的。其中的安全活性成分,耐受性好,无副作用,保证了非转基因的特性,适合素食者和严格素食者,为大众的消化道健康开启了新的疗法。
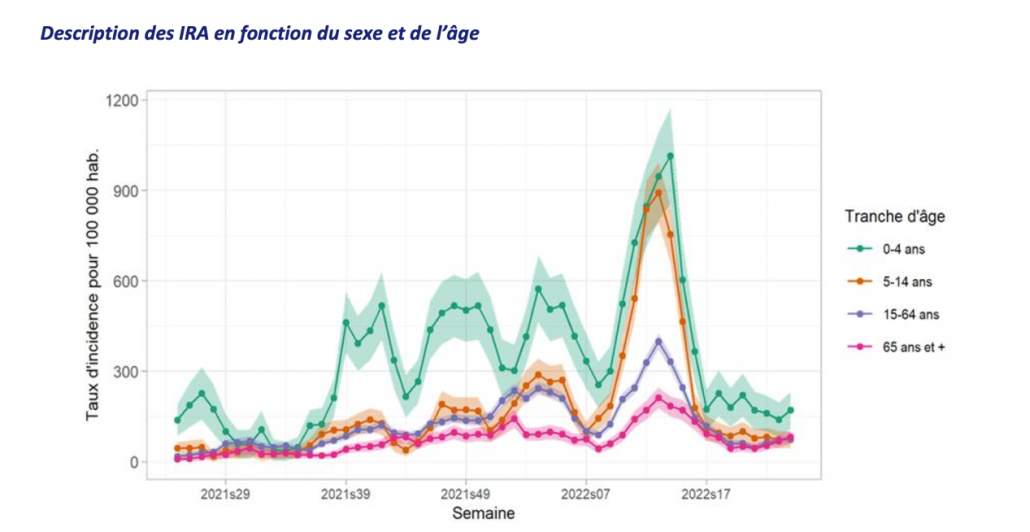
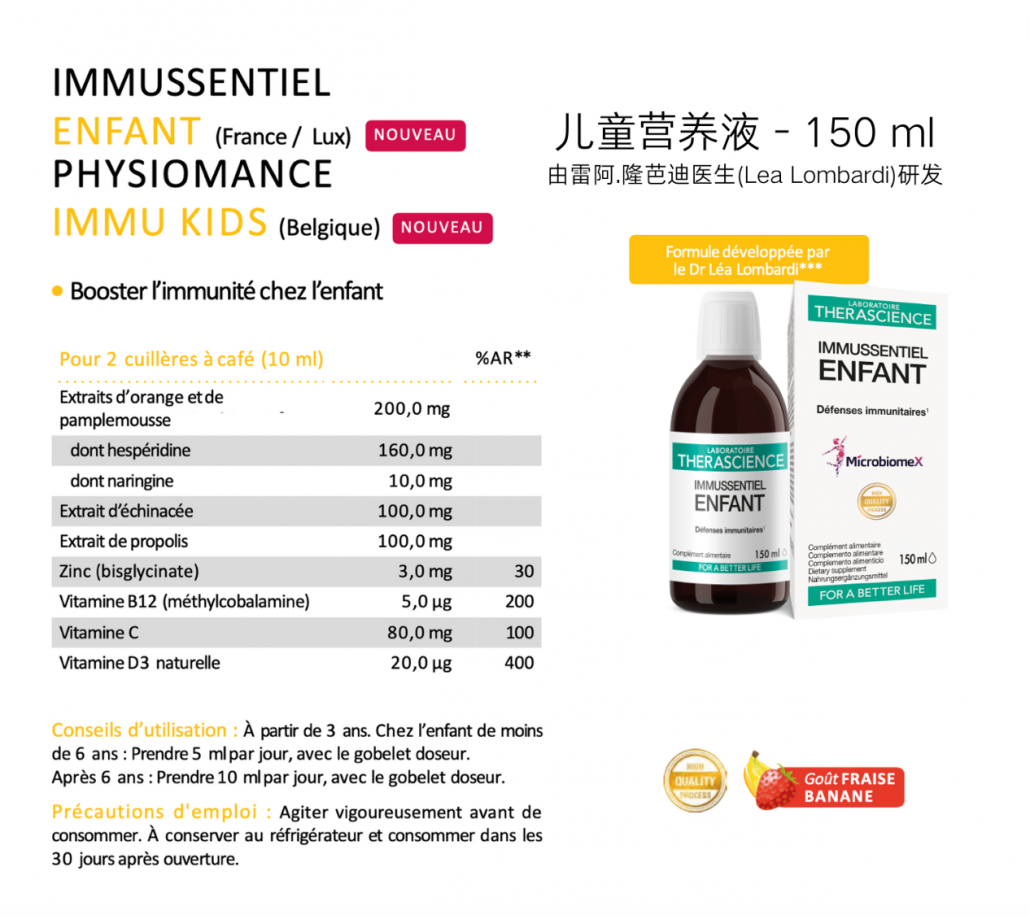
同时数据显示,法国急性呼吸道疾病感染较多的是0-4岁和5-14岁这两个年龄段,这和青少年免疫力薄弱有一定关系。雷阿.隆芭迪医生(Dr Lea Lombardi)研发也针对儿童推出了含有多项专利成份的益生菌和后生元综合营养素。
布鲁诺,布纳斯医生(Pr Bruno BONAZ)是法国格勒诺布尔医院肝肠科医生,同时是脑神经研究院专家(Grenoble Institut des Neurosciences),他分析和讨论了脑-肠轴最新的研究和数据. 提供了新冠和流行病后康复重要的临床学术和科学研究支持。
安娜玛丽教授(Anne marie ROUSSEL)针对长期慢性新冠后遗症,以及相关的老年人智力衰退进行了讨论。推出了针对老年人神经保护的Neuron和炎症的Resolvines营养素。
Jacque Bassier 医生也关注了青少年短期考试对记忆力以及专注力的需求,推出了Jeuron的青少考试期间营养素。

参考文献:
1.Postbiotics and Their Potential Applications in Early Life Nutrition and Beyond
2.Scavenger receptor for lipoteichoic acid is involved in the potent ability of Lactobacillus plantarum strain L-137 to stimulate production of interleukin-12p40.
3.Rational identification of diet-derived postbiotics for improving intestinal microbiota function
4.Probiotics for Gastrointestinal Conditions: A Summary of the Evidence
痤疮
多年来,临床、流行病学、激素、分子和实验数据的结合使得将 痤疮 视为一种雄激素依赖性病症成为可能。青春期痤疮是全身雄激素过多症或毛囊皮脂腺对循环雄激素过敏的同义词。青少年痤疮逐渐成为一种慢性疾病,涉及皮肤病学、内分泌学、感染学、营养学、心理学以及最近的环境污染。
新概念丰富了青春期这种慢性致残疾病的病理生理学,在 14 至 16 岁之间出现高峰。痤疮仍然经常被认为是一种附带现象,是伴随青少年青春期开始的必要通道。大约 70% 至 90% 的青少年患有痤疮病变,其中 25% 至 70% 需要积极的医疗或辅助医疗护理。此外,最近的流行病学数据表明痤疮的增加令人担忧。后者被认为是西方文明的疾病。此外,在饮食变得西化的群体/种族中,青少年痤疮的患病率增加。
当建立性别化的身体形象时,它对青春期变态的影响程度会影响生活质量,并在某些情况下产生真正的畸形恐惧症。通常,青春期结束时痤疮会自发消退,但有 10% 至 20% 的病例会在 20 岁以后持续存在。这种真正的障碍将影响个人的日常生活、心理、社会、学校和大学生活。
然而,目前有很好的治疗选择,最近发现了与青春期痤疮发展有关的几个因素,进一步丰富了这些选择。
痤疮主要影响面部(前额、下巴、脸颊、鼻子),但也可以在背部、胸部、…
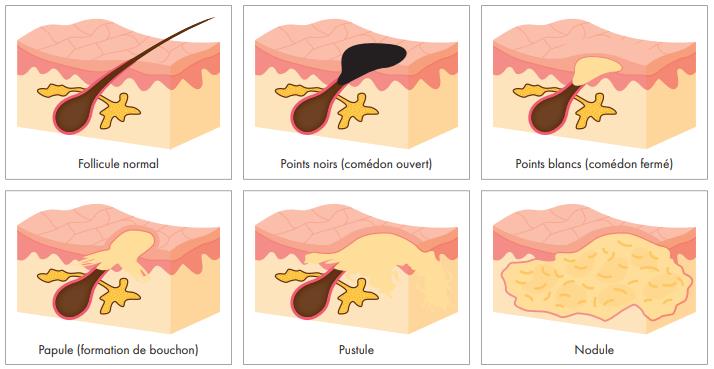
我们通常区分不同的临床表现(图1):
- 第一阶段:粉刺性或保留性痤疮,以黑头和白色粉刺为特征;
- 第 2 阶段:炎症性痤疮,由微囊(红色和白色丘疹)组成;
- 第3 阶段:丘疹脓疱性痤疮,具有主要的炎症反应和结节的存在。
根据痤疮的严重程度,可以分类如下:
- 轻度,< 20 个粉刺和/或< 10 个炎性病变;
- 中度,< 100 个病灶
- 重度粉刺、炎性病变和囊肿的关联。
根据 2018 年在 EADV* 上发表的一项研究,对 1,000 名痤疮患者(包括 85% 的年轻人)进行的研究为轻度或中度痤疮。
最近,沙特阿拉伯的一项流行病学分析报告了 65% 的青少年出现轻度和中度痤疮的频率。 应该指出的是,其中 30% 的 BMI ≥ 30,继发于饮食过量7。
- 对双胞胎进行的分析表明,痤疮的遗传表现得到了直系亲属的证实。毫无疑问,青春期痤疮的发展存在遗传易感性。对人类基因组的分析揭示了 15 个位点,其中包含 3 个参与毛囊皮脂腺发育的基因。
- 还需要具体说明社会经济水平、生活方式和饮食习惯(定量和定性):西方饮食使痤疮的风险增加。
- 最后,有必要询问痤疮对“青少年”心理平衡的影响程度(甚至轻微)。在我们的形象社会中,青少年的识别集中在那些模特完美面孔的照片上,光面纸模特,痤疮,甚至轻微的,都有影响自尊和自尊的风险。导致心理障碍,甚至可能导致抑郁。
生理病理学新概念
五个主要因素在痤疮的病理生理学中起决定性作用:
- 皮脂腺分泌的皮脂增加;
- 毛囊角质化过度和随后的毛囊滞留;
- 皮肤上的细菌定殖;
- 局部炎症;
- 皮脂腺对雄激素的依赖。
1.皮脂腺:调节因素
皮脂细胞的分化、增殖和脂质合成主要受内分泌因素的调节。请记住,毛囊皮脂腺既是内分泌腺,也是几种激素的靶组织。
雄激素:二氢睾酮 (DHT),通过 5-α 还原酶还原睾酮,睾酮由生殖器官产生或由肾上腺雄激素原位产生(尤其是硫酸 DHEA)。 SDHA 的增加发生在肾上腺功能亢进期间,这是青春期开始之前的发育阶段。 30 多年前,我们在痤疮区域的“穿刺活检”中报告说,痤疮是由于皮脂腺的 5-α 还原酶过度活跃11。此后,多项研究证实了这些原始数据。
IGF-1:这种生长因子受生长激素的调节。它的增加伴随着青春期的生长突增。在激活 PI3K/AKT 和 MAPK/ERK 转导通路后,IGF-1 通过诱导 SREBP-1 刺激皮脂生成。
FGF(及其受体),其分泌受雄激素刺激,激活角质形成细胞的增殖。
微 RNA:调节基因表达的非编码 RNA。例如,mi-RNA 574 的超表达增加了皮脂腺中的脂质生物合成。
神经肽:皮脂腺有 CRH、黑皮质素、β-内啡肽、神经肽 ϒ 等受体。
脂肪因子:据IL-6、瘦素、抵抗素、维他汀参与毛囊皮脂腺的调节。
如果说雄激素的作用长期以来被认为是痤疮发展的关键因素,那么新的概念已经出现,以完善对青春期痤疮出现机制的理解:
- 暴露
- 皮肤微生物组
- 皮肤,代谢综合征的参与者
2. 暴露
暴露体由人类从胎儿生命到死亡所暴露的环境、营养、行为和激素因素的组合来定义。 暴露体调节痤疮的发持续时间和强度。
涉及痤疮发展的暴露体的主要成分是营养、药物、生活方式、气候因素、环境污染、心理问题和内分泌平衡。
- 营养:过去经常引起争议,营养质量已成为青春期痤疮发展的主要因素。正是西方饮食,通过其丰富的乳制品摄入量、高血糖指数的碳水化合物和脂肪酸……产生了相当大的影响。还需要强调某些膳食补充剂,富含亮氨酸,与痤疮的出现有关。
- 药物:许多药物与青春期痤疮的发作有关:抗癫痫药、合成代谢类固醇。
- 生活方式:压力和情绪是促进青春期痤疮出现的因素,此外还有社会经济压力。最后,吸烟通常被认为是一个危险因素。
- 涉及到的气候因素:高温、空气湿度、紫外线。
- 环境污染最近已成为痤疮发展的一个因素。二恶英(一种强力杀虫剂)、多环芳烃起到一定的作用。化妆品也是如此,因为它们含有内分泌干扰物。
- 心理问题通常是痤疮对身体形象的影响;它们导致青春期危机伴随而来的心理困难。
- 激素:青春期出现生理性雄激素过多症。这种高雄激素血症在某些情况下会加剧,例如超重和随后的高胰岛素血症。
3. 微生物组
微生物组包括所有共生微生物、细菌、病毒和真菌、它们的代谢物和化学环境。 在痤疮中,微生物组包括:
- 痤疮角质杆菌(原痤疮丙酸杆菌)
- 表皮葡萄球菌
微生物失衡或生态失调已成为与痤疮相关的炎症的病理生理学相关的一个新因素。 最近的数据强调,除了痤疮皮肤杆菌的浓度,痤疮皮肤杆菌系统型的多样性缺乏。 最近已知许多皮肤激素以及神经激素可以调节细菌的作用。 最近,已经报道了儿茶酚胺(肾上腺素、去甲肾上腺素、多巴胺)对微生物组的作用,强化了最近微生物内分泌学的概念。 最后,微生物组不仅参与刺激过度皮脂溢出、角化过度、感染,而且还有助于产生聚集皮脂的生物膜。
4. 皮肤,代谢综合征的参与者
经常有争议的是,营养在痤疮发展中的作用已通过分子机制的阐明得到明确证实,这为营养与痤疮的关系提供了新的视角。
mTORC 是 PI3K 家族的丝氨酸/苏氨酸激酶,可根据能量水平、生长因子和营养摄入量调节细胞生长、细胞周期。 外源因子(蛋白质、脂质、碳水化合物)激活 mTORC1 导致细胞生长和合成代谢。 mTORC 的激活将促进皮脂腺脂肪生成。 此外,mTORC 与肥胖和胰岛素抵抗的发展有关。
痤疮应该选择的营养成分
荨麻
自古以来就为人所知和使用,这种植物含有蛋白质(8 种必需氨基酸)、钙、铁、镁、锌、锰……还有维生素(A、B1、B2、B5、C)、多酚……
除其他外,荨麻在治疗痤疮方面具有两个基本特性:
- 抗炎作用,其基于抑制环加氧酶、脂加氧酶、细胞因子 (IL-1β) 和核因子 Kβ 的产生。
- 抗糖尿病作用:通过刺激胰岛素分泌,具有降血糖作用。 该活动通过减少肠道对葡萄糖的吸收和朗格汉斯胰岛的营养不良来完成。
锯棕榈
锯棕榈(Serenoa repens)主要生长在佛罗里达州,自 19 世纪以来,美洲原住民(居住在美国东南部的该州)曾经使用它来治疗前列腺良性肥大的功能症状。
它由游离脂肪酸、酯化脂肪酸、月桂酸、油酸、肉豆蔻酸、棕榈酸组成……其作用机制有两个:
- 一种抗炎作用21,可抑制 PG 合成酶和 5-脂氧合酶的活性并减少 IL-1β 和 TNF-α 的产生。此外,锯齿棕通过下调参与该反应的某些因子来减少白细胞浸润。
- 抗雄激素作用:30 多年前,我们强调了锯齿棕 B 的作用机制:通过抑制培养的人包皮成纤维细胞 5-α 还原酶的活性,锯齿棕 B 首次作为一种抗雄激素,通过减少 DHT(靶组织中的活性雄激素)的产生 22。随后,Bayne 等人。证实,在前列腺腺瘤细胞培养物中,5-α 还原酶 1 和 223 的抑制作用。Raynaud 等人的团队。通过证明锯齿棕 B 中存在的游离脂肪酸增强了 5-α 还原酶的抑制作用,强化了这些数据。同样有趣的是,锯齿棕能够结合雄激素受体(部分拮抗剂)22, 25。
芦荟
- 维生素:A、C、E、B12;
- 减少炎症的酶;
- 矿物质:钙、铜、……,参与酶活性;
芦荟是属于Asphodelaceae 阿福花科家族的植物。 它包含不少于 75 种活性化合物:
- 抗炎蛋白;
- 蒽醌类:镇痛药;
- 氨基酸:8 种必需氨基酸中的 7 种。
芦荟是“大自然赐予的神奇礼物”,同时具有抗氧化、抗菌、抗病毒、抗炎和免疫调节作用,同时还能保护皮肤。作用机制:
- 抗炎:抑制环氧合酶途径并减少PGE2 的产生;
- 免疫:它刺激IL-1 / TNF-α的产生(含氧自由基的释放);
- 防腐(抗菌)。
α-硫辛酸
它是一种由某些植物产生的有机硫化合物,它是丙酮酸脱氢酶和α-酮戊二酸脱氢酶的辅因子等。 它也是一种直接或间接的抗氧化剂,一种强大的重金属螯合剂。
α-硫辛酸有 5 种主要活性:
- 通过加速细胞内胰岛素的转导来降血糖,改善 OGTT 期间的胰岛素峰值;
- 抗炎:NF-Kβ;
- 抗氧化剂:降低氧化应激;
- 解毒;
- 抗菌(针对痤疮丙酸杆菌)。
锌
锌是一种二价阳离子,参与大约 300 种金属酶和 2000 种转录因子的活性。因此,它在个人的成长和发展中起着至关重要的作用。它通过核受体的 DNA 结合域和表观遗传机制,通过组蛋白的去乙酰化参与基因转录的调节。在患有痤疮的年轻人中,血清中的锌浓度会降低 。
它在护理中的作用可以分为两个层次
- 炎症反应:
- 它通过减缓 IL-6 和 TNF-α 的产生来抑制炎症过程
- 减少一氧化氮的产生
- 减少感染痤疮丙酸杆菌的角质形成细胞产生整合素
- 减少痤疮丙酸杆菌增殖
- 抑制NF-kβ介导的信号通路
- 雄激素依赖:
- 减少体内皮脂分泌
- 在体外,它通过非竞争性抑制 T 与 5-α 还原酶的结合以及减少 NADPH 辅助因子的形成来抑制 5-α 还原酶活性。
它下调雄激素受体的表达,从而降低雄激素在靶细胞水平上的转录活性,例如皮脂腺。
文章来源:https://iepp-eu.com/wp-content/uploads/2013/04/IEPP-Lettre-n36-ACNE-VDOC1004_HD.pdf
非酒精性脂肪肝病
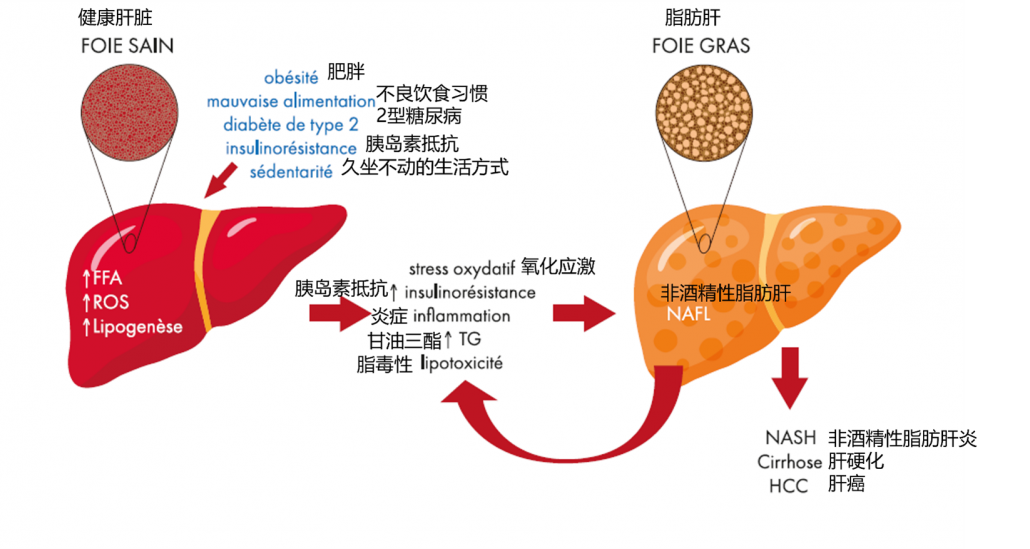
脂肪超负荷肝病,通常被称为“苏打病”或“脂肪肝病”,在没有过量饮酒的情况下,现在是西方慢性肝病的主要原因。
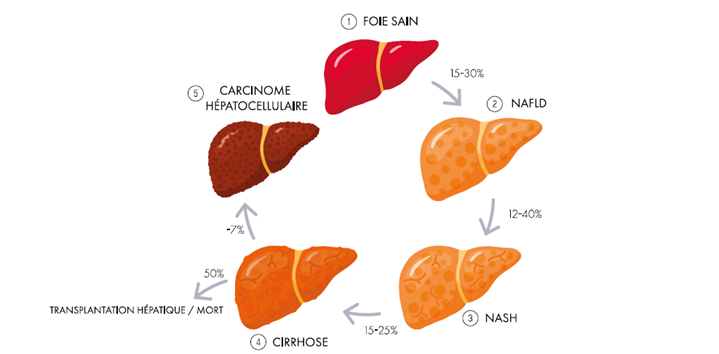
作为具有营养和环境成分的代谢疾病,这些病理范围从简单的非酒精性脂肪变性(NAFLD 或非酒精性脂肪肝病)到非酒精性脂肪性肝炎(NASH 或非酒精性脂肪肝炎),如果及时治疗是可以乔雅登。 酒精性脂肪性肝炎,可发展为纤维化和肝硬化、严重且不可逆的病症。
非酒精性脂肪肝病的特征是至少 5% 的肝细胞中甘油三酯异常积聚。它通常在没有明显临床症状的情况下发展。它与肥胖和代谢综合征密切相关,并且与心血管发病率和死亡率的增加独立相关。
非酒精性脂肪肝病作为流行病影响所有国家。在法国,它影响了超过 20% 的人口,包括越来越多的青少年和年轻的超重受试者1-2。
在 12% 至 40% 的病例中,非酒精性脂肪肝病发展为非酒精性脂肪肝炎,这强调了实施早期筛查和管理的重要性。
由于迄今为止提出的各种药物治疗仅显示出有限的功效,因此生活方式和饮食措施的实施,包括使用适当的营养补充剂,至今仍是一种值得青睐的管理方法。
非酒精性脂肪肝病的发病机制很复杂,部分原因尚不完全清楚。
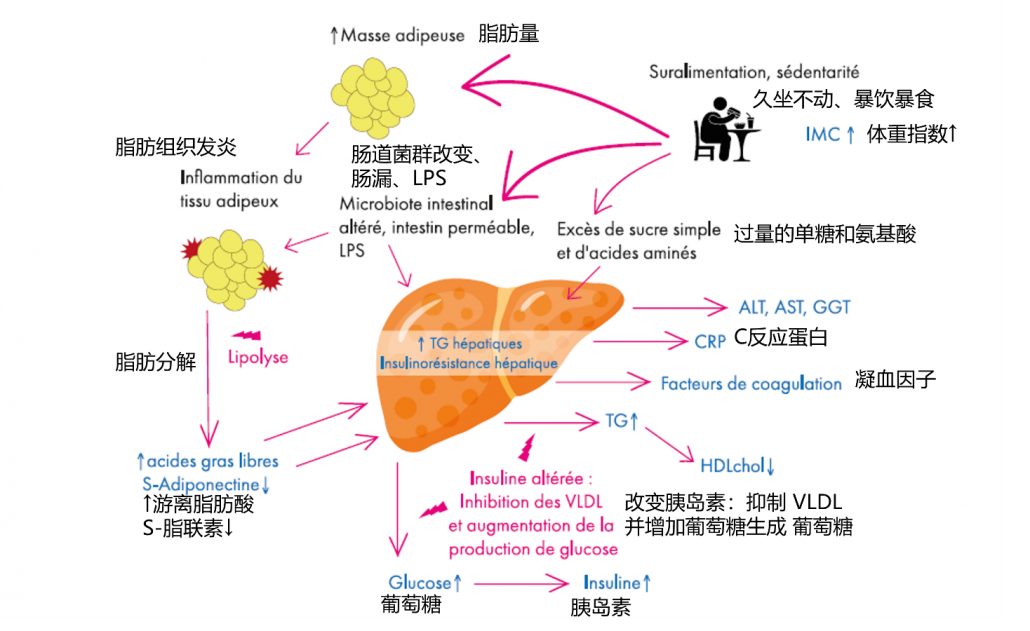
肥胖、胰岛素抵抗、高血压、高胆固醇血症和高甘油三酯血症等代谢综合征特征是非酒精性脂肪肝病发生的主要成分。事实上,肝脂肪变性和胰岛素抵抗之间的相互作用似乎是非酒精性脂肪肝病发展的两个关键因素,但很可能还有一个遗传因素导致非酒精性脂肪肝病的易感性与增加风险的遗传多态性有关。胰岛素抵抗和脂肪肝。
多因素机制导致非酒精性脂肪肝病中遇到的代谢功能障碍和生物参数紊乱。因此,报告了过度消耗食物和久坐的生活方式、果糖摄入、尿素循环紊乱、微生物群改变和线粒体功能障碍的作用。
过度饮食和久坐不动的生活方式会导致脂肪组织扩张、缺氧和巨噬细胞浸润脂肪细胞。脂肪细胞的浸润诱导促炎细胞因子如 TNF- 和趋化因子如单核细胞趋化蛋白 1 的产生。这种炎症情况导致脂联素缺乏并促进游离脂肪酸的释放。
甘油三酯在肝脏中的积累是脂肪组织中游离脂肪酸流入的结果,也是它们合成增加的结果,以及原位甘油三酯输出的减少酸-氧化。
肝内脂质的积累会干扰细胞内胰岛素信号通路并维持肝胰岛素抵抗。
在所有情况下都存在胰岛素抵抗:
- 增加脂肪组织中甘油三酯的脂解作用,这是脂质过氧化的来源并增加促炎细胞因子的产生。
- 激活脂肪酸的重新合成,
- 增加肝内甘油三酯的储存,
- 减少极低密度脂蛋白的分泌和输出.
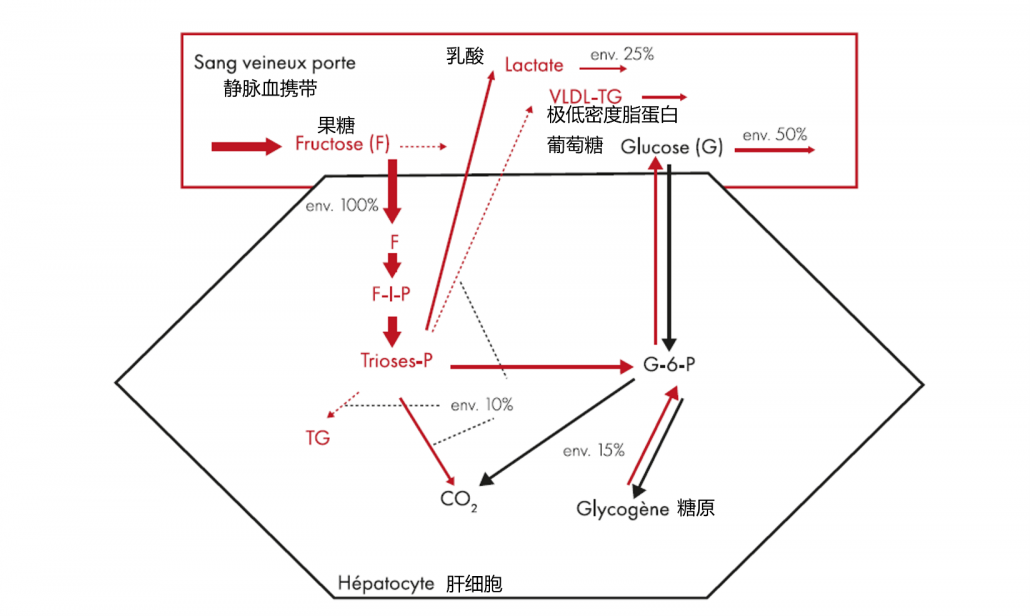
过量摄入果糖和添加糖:
适度消耗(<50 g/d),果糖参与能量代谢和产热。 然而,过量时,它会诱导肝细胞的脂质超载。
在过去的几十年里,随着食品工业的发展,我们对果糖的消费量显着增加。 由玉米淀粉工业制备的高果糖糖浆存在于苏打水和许多工业食品中。 在西方饮食中,果糖和添加糖的摄入量估计超过 80 克/天,平均达到我们能量摄入量的 15%,对于青少年、年轻人和某些少数民族(太平洋岛屿、非洲美国人、南美洲人)
果糖的代谢不同于葡萄糖。 果糖的过量和长期消耗会导致肝细胞脂质超载,因为肝磷酸果糖激酶 C 对果糖的代谢会刺激脂肪酸的从头合成,阻止它们的氧化并降低能量消耗 。
同时,ATP的产生减少。 肝脏 ATP 产量的下降会引发一系列反应,包括氧化爆发、肠道通透性增加和线粒体功能障碍。
几种饮食因素会加剧非酒精性脂肪肝病的诱发:高脂肪、高盐、高血糖指数食物和酒精的饮食。
尿素循环中断和高氨血症:
肝脏是氨解毒的场所。 大多数氨基酸在肝脏中代谢,参与糖异生,或通过尿素循环和 NH4 产生排出体外。
在非酒精性脂肪肝病中,尿素循环酶的表达降低,导致肝毒性高氨血症。 因此,尿素循环和氨的调节是肝纤维化预防性治疗的目标。
微生物群改变:肠道通透性、细菌易位和肝脂肪变性之间的联系
通过肠通透性、细菌易位和肝脂肪变性之间的相关性,肠/肝轴与非酒精性脂肪肝病密切相关。 因此,在增加肠道通透性和肠道细菌易位的生态失调中,LPS 等化合物的产生及其通过门静脉向肝脏的迁移参与脂肪细胞和非酒精性脂肪肝病的肝脏炎症。
在微生物群的紊乱中,小肠最近被描述为与非酒精性脂肪肝病的密切相关。
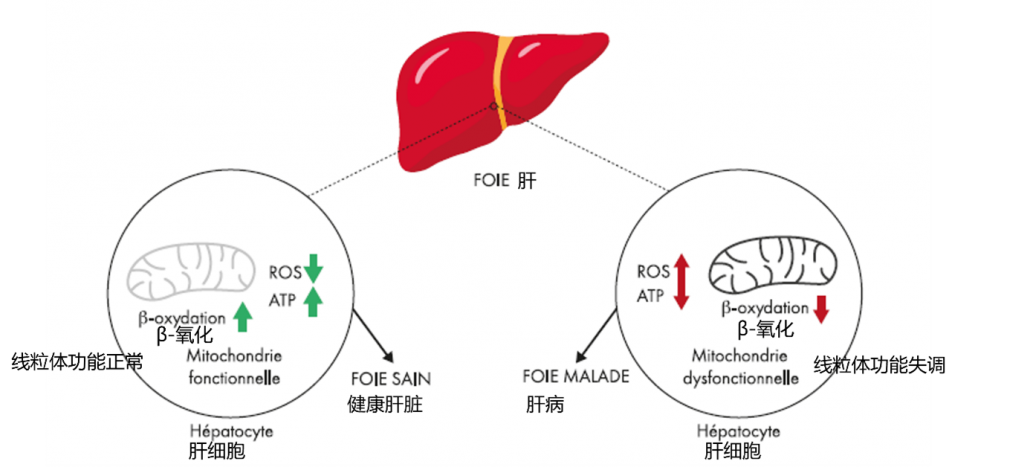
线粒体功能障碍
在 非酒精性脂肪肝病中,线粒体的生物发生和功能下降导致其氧化脂质的能力下降。 抑制-氧化和降低柠檬酸合酶 (CS) 活性会导致柠檬酸循环减慢、呼吸链复合物的活性降低和 ATP 的产生,以及产量的增加的激进物种。
生物自由基参数因此被修改,脂质和碳水化合物血浆分布失调。
通过生物活性化合物和微量营养素管理非酒精性脂肪肝病和非酒精性脂肪肝炎
与游离脂肪酸的流入和储存在肝脏中引发炎症氧化过程和线粒体毒性有关,这些具有强烈营养成分的疾病及其相关风险必须及早处理。
在没有证明其有效性的预防性药物治疗的情况下,治疗必须是:
- 通过卫生和饮食建议,这在任何治疗中都必不可少:减少热量摄入、减轻体重、反对久坐的生活方式、停止含有果糖的含糖饮料、坚持地中海饮食、定期进行体育锻炼等。
- 通过适当的补充:一些生物活性化合物和微量营养素已在临床上显示出它们对治疗非酒精性脂肪肝病的作用。
1. L-鸟氨酸-L-天冬氨酸盐(LOLA)
口服后,盐解离成 2 个组成氨基酸:L-鸟氨酸和 L-天冬氨酸,它们通过主动转运被吸收、分布和代谢,产生谷氨酰胺、谷胱甘肽和一氧化氮。
这些代谢物的产生解释了 L-鸟氨酸-L-天冬氨酸盐在慢性肝病中的保肝作用。
补充剂的保肝特性最近已在人体中得到临床证实,涉及:
- 谷胱甘肽的抗氧化和解毒特性,由鸟氨酸通过转氨作用生成谷氨酸。
- 通过增加从L-鸟氨酸、然后是L-精氨酸产生的一氧化氮来激活微循环。
- 谷氨酰胺的解毒作用增加了肝脏对尿素循环或谷氨酰胺合酶中过量NH4 的解毒能力。
LOLA补充剂的临床益处:
AST、ALT 非酒精性脂肪肝病组的效果比肝硬化组更明显,结果由第二项研究证实报告在补充 12 周后 ALT 和甘油三酯显着下降,并且通过断层扫描测量肝脏和脾脏显着改善 。
最后,在最近一项对 78 名非酒精性脂肪肝炎患者进行的试验,补充剂可改善肝脏微循环。
2. LA SILYMARINE 水飞蓟素
从水飞蓟 (Silybum marianum) 中提取的水飞蓟素是一组多酚类物质(水飞蓟宾 A 和 B、异西比林、水飞蓟素、水飞蓟素、异水飞蓟素和紫杉叶素)。 在所有这些化合物中,水飞蓟宾以最具生物活性的形式存在最多。
保肝特性和机制:
水飞蓟素通过抑制 Kupffer 细胞中 LT4 白三烯的形成而起作用,减轻炎症,并通过抑制纤维化诱导基因(如前胶原-和 TGF-)的表达,减少纤维化并刺激肝脏再生。
此外,它具有抗氧化和膜稳定活性,降低胰岛素抵抗并激活胆汁排泄。
补充的好处:
在 138 名非酒精性脂肪肝病患者中,摄入水飞蓟素(188 mg/d)12 个月,结合胆碱和维生素 E,使转氨酶正常化,减少 -GT,改善胰岛素抵抗和逆转脂肪变性。
在另一项与安慰剂比较的临床研究中,180 毫克/天的水飞蓟素 3 个月改善了非酒精性脂肪肝病患者患者的生物特征参数:腹围、BMI 和肝脏的组织学分析。 对 8 项研究和 587 名患者的荟萃分析证实了水飞蓟素对非酒精性脂肪肝病患者治疗效果。
3. 谷胱甘肽、乙酰谷胱甘肽和N-乙酰半胱氨酸
谷胱甘肽在调节自由基氧的产生和肝脏解毒中起着核心作用。 谷胱甘肽(L-谷氨酰-L-半胱氨酰甘氨酸)缺乏是肝细胞对氧化应激和细胞因子诱导的细胞死亡敏感性进展的主要因素之一。 在非酒精性脂肪肝病患者中观察到氧化爆发(增加 MDA、ox-LDL、TAC、SOD、GPx)和谷胱甘肽消耗。
口服谷胱甘肽通过刺激 PPArs-受体,增加脂肪酸的利用,降低血浆中游离脂肪酸、甘油三酯、铁蛋白和 ALAT的水平。
众所周知,补充谷胱甘肽或其前体 N-乙酰半胱氨酸对慢性肝病的益处。
S-乙酰谷胱甘肽 (S-GSH)
血液中 GSH 的寿命很短,这限制了其被细胞吸收。 通过使用具有更高稳定性和更好生物利用度的 S-乙酰谷胱甘肽 (S-GSH) 形式可以避免这一障碍,这种形式在被细胞吸收后直接转化为还原型谷胱甘肽。
N-乙酰半胱氨酸(NAC)
N-乙酰半胱氨酸是公认的谷胱甘肽前体,在 NAFLD 的管理策略中占有一席之地。 在人类中,NAC/二甲双胍组合可显着减少肝脂肪变性和纤维化。 最近的一项研究报告了补充NAC 3 个月(600 毫克/天)对 ALT 水平和脾脏大小的有效性 。
4. 熊果酸
熊果酸是一种五环三萜,具有抗炎和抗氧化、保肝和预防脂肪变性和代谢综合征的特性:调节脂肪生成、脂肪酸氧化、胰岛素抵抗、线粒体、糖异生、氧化应激和炎症。
熊果酸的几种作用机制:
- 碳水化合物稳态的调节:GLUT4 的易位和抑制淀粉酶和减少淀粉吸收,抑制果糖代谢。
- 降低甲基乙二醛的细胞毒性并刺激乙二醛酶系统。
- 减少脂肪细胞的分化
- 刺激线粒体脂肪酸氧化。
在动物模型中,熊果酸可减轻脂肪肝、纤维化和胰岛素抵抗
在人类中,熊果酸 150 毫克/天,持续 3 个月,可调节体重、胰岛素敏感性和血糖,并促进肝脏解毒 。
5. 非维生素 A 类胡萝卜素:番茄红素的好处
具有非维生素 A 原活性的类胡萝卜素在预防和治疗非酒精性脂肪肝病方面的潜力已被广泛报道,最近也有文献记载。
非酒精性脂肪肝病患者的血浆番茄红素水平较低,相反,高水平与非酒精性脂肪肝病的改善和 TG、HOMA-IR 和 BMI 降低有关。
最近证明,除了所有类胡萝卜素共有的抗氧化和抗炎作用外,摄入番茄红素对肝脂肪变性的益处还在于减少了编码脂肪生成基因(如 SREBP-1)的表达。
6. LA CHOLINE47-48胆碱47-48
胆碱是一种必需营养素,其代谢发生在肝脏中,其缺乏会伴随肝脏脂肪变性和肝细胞死亡。
胆碱的肝脏代谢通过磷脂酰胆碱形式,这是 极低密度脂蛋白中甘油三酯的输出和胆汁盐溶解所必需的。
在胆碱缺乏症中,观察到的肝脏疾病的起源有多种机制:甘油三酯合成异常、极密度脂蛋白分泌受损、线粒体功能障碍和氧化应激、肠道微生物群的干扰。
由于 极低密度脂蛋白输出的改变是脂肪变性的核心,胆碱需求的覆盖似乎对于预防脂肪变性至关重要。 在患有脂肪变性的受试者中,一项大型研究(>56,000 名患者)报告了 NAFLD 的出现与胆碱摄入量之间的反比关系。
总结
- 非酒精性脂肪肝病是一种日益流行的疾病,包括在儿童和青少年中。
- 任何患有代谢综合征、肥胖症、2 型糖尿病、肝功能检查异常或有心血管疾病病史的患者都应筛查非酒精性脂肪肝病。
- 生活方式和饮食措施以及生态失调的治疗构成了具体治疗的初步基础。
- 应尽早实施适当补充生物活性化合物,这些化合物已在发病机制的不同阶段显示出临床和生物学功效,目的是减少脂肪变性和使肝功能测试正常化。
文章来源 https://iepp-eu.com/wp-content/uploads/2013/04/IEPP-Lettre-n35-NASH-VDOC973-202009.pdf
Therascience益生菌进入中国市场 获得摩纳哥2021商务部经济和创新奖项
Therascience益生菌进入中国市场 获得摩纳哥2021商务部第10届经济和创新奖项
日前,第10届摩纳哥商务部(MonacoEconomicBoard)为七家公司颁发了创新和经济奖项,经济部部长皮埃尔.达图(PierreDartout)指出,这些公司捍卫了摩纳哥大公国在新冠疫青期间面对危机而展现出来韧劲。
Therascience获得了创新和数字奖项,文章指出:让-皮埃尔·阿加拉 (Jean-Pierre Agarra) 是一位远见卓识的企业家:从1998年建立以来,他深信营养和食品补充剂对我们的健康有益。
Therascience实验室拥有 500 多种产品,现在是欧洲食品补充剂专业市场的领跑者之一。让-皮埃尔·阿加拉总裁说,Therascience与法国国家科学研究院(CNRS)、法国国家农业研究院(INRA)和法国国家医学和健康研究中心(INSERM)等组织建立了紧密的研发伙伴关系;并且与大学教授、研究人员、医生、药剂师等科学专家深入合作。研究和持续创新是 Therascience 实验室的企业基因。在其研究方向中,2023将新增十多个品种,现有配方会根据前沿科学研究持续改进。
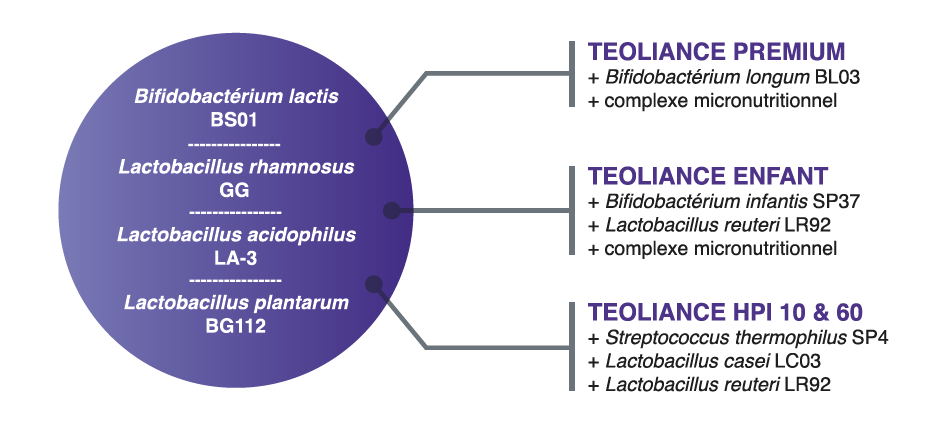
Therascience 实验室在1999年推出第一款益生菌产品,目前有Immu 5, Enfant, Immu 10, Premium, Intima, HPI 10, HPI 60, Trisymbio,Oral, 2’-FL, Activ’ 等多款益生菌菌产品, 在欧洲法语地区(法国、瑞士、比利时、卢森堡、摩纳哥)以及意大利的药店及医疗渠道销售 ,在中国除了用跨境电商销售,还推出四款中国线下市场的益生菌, 德诺海科悠乐,德诺海科舒乐,德诺海科舒源,德诺海科悠源。
此外,摩纳哥物流公司(Monaco Logistique)获得最佳经理人奖项,摩纳哥港口管理公司 (Societe d’Expoloitation des Ports de Monaco)通过开拓北美市场也获得管理大奖。
文章指出,由于摩纳哥位于地中海蔚蓝海岸,高净值客户多,富人集中,所以对产品质量以及服务要求也高,现在欧洲疫情没有结束,这些企业的创新,管理的精神代表了摩纳哥的不断发展和进步的价值。
Therasicence 抗衰老系列
由于高净值人群近20年对延长生命以及精力体力不断的要求,Therascience德诺海科的明星 抗衰老系列 CELLSSENTIEL 2020年升级成为CELLEXTENSE 不断研发扩充系列,目前包含10款产品,其中根据诺贝尔奖的NADH+还原型烟酰胺腺嘌呤二核苷酸, PQQ(醌吡咯并喹啉),是大众熟知的明星产品,针对国际市场的NMN。
德诺海科Therascience总部位于法国南部接壤的摩纳哥Monaco,是全球富人集中的国家,连续多年房产超过中国香港,瑞士日内瓦价格全球蝉联第一,公司成立22年,产品欧洲高标准制造,纯天然,安全,明显的效果得到了欧洲法语区高净值人群的青睐(摩纳哥,法国,卢森堡,瑞士,比利时),被誉为保健品类的“奢侈品牌”。
德诺海科Therascience首席科学家Anne-Marie ROUSSEL 在国际论坛讲述产品机理
Anne Marie ROUSSEL在学术会议上解释产品机理以及成份配比
抗衰机理
从诺贝尔, 衰老的发展过程与线粒体功能异常有密切关系。在衰老过程中, 线粒体生物学发生变化, 线粒体产生自由基和自由基对线粒体的损伤对衰老的发展起到促进作用; 线粒体 DNA 突变和线粒体对细胞死亡进程的调控与衰老的进程有密切关系。 线粒体是细胞有氧呼吸和合成三磷酸腺苷(ATP)的主要场所,为细胞的活动提供了化学能量,所以有“细胞的发电站”之称。除了为细胞供能外,线粒体还参与诸如细胞分化、细胞信息传递和细胞凋亡等过程,并拥有调控细胞生长和细胞周期的能力。
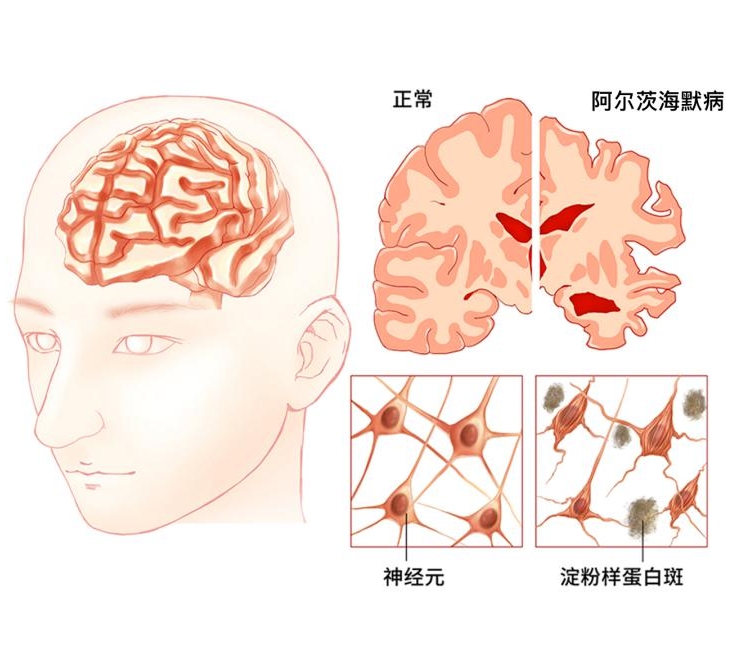
衰老伴随着所有组织中线粒体功能的普遍下降,线粒体受损,身体和神经系统都会受到不同程度的影响,主要表现为:皮肤松弛、脱发、精力不济、记忆力衰退、失眠等,甚至导致神经退行性疾病。
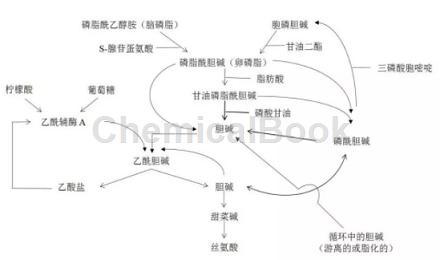
科学家发现,有一种被称为线粒体素NADH的物质(化学名称:还原型烟酰胺腺嘌呤二核苷酸)它是存在于人体细胞内一种生物形式的氢。NADH进入体内后能够高效分解为NAD+和氢,这样既提升了NAD+水平,氢也正是能够高效清除自由基的最理想物质。中国著名呼吸病学专家、中国工程院院士钟南山曾说:“鉴于氢分子具有很强的抗氧化作用,特别其高选择性(仅中和毒性活性氧自由基)、高弥散性和高安全性,因此受到广泛重视”
只要提高了细胞中线粒体素NADH的含量,细胞就能生产足够的、生命所必须的能量,进而可以更好发挥细胞的各项功能。
心脏和大脑是所有器官中最需要线粒体素NADH的,所以这些器官通过外源补充线粒体素NADH获得的收益最多。其他器官,特别是肺、肝、肾等,也要通过补充线粒体素NADH从而获取较多能量,才能更好的发挥功能。
服用NADH后,体内NAD+的水平
NAD+是细胞中含量最丰富的辅酶,而NADH作为它的还原形式。在呼吸作用中,在糖酵解、三羧酸循环过程中由NAD+产生NADH,而在氧化磷酸化过程中,NADH释放出质子和电子,提供能量合成ATP,并自身被氧化为NAD+。
世界上最早的国际顶级学术刊物之一《自然》(Nature)杂志在2019年10月刊登了一份最新研究,介绍了诺加因子NADH对疾病干预与抗衰功效的科普。NAD+ 和NADH , NADH是NAD+的还原态,直接参与线粒体ATP的能量合成。1粒NADH+胶囊大约相当于4粒NMN胶囊,这也是NMN为什么普遍计量要大于NADH+,因为在吸收和转化中容易流失。
NADH对光线和空气里的水分特别敏感。而且在进入胃部后极易被降解,极不稳定。由于上个世纪的技术条件尚未达到,大多数神经退行性疾病患者都是通过注射的方式进行治疗。德诺海科实验室Therascience的明星产品NADH+产品专利技术,以及创新的反式胶囊技术,保证不受胃酸影响,显示出温度和易吸收的特性。这款产品不仅含有诺奖获得者亚瑟・哈
和比克麦尔教授不懈努力的成果NADH,还含有维生素B1。NADH刺激神经递质的自动合成,与维生素B1的协同作用:强化神经系统,调节压力,集中注意力,增强记忆力。能有效预防由衰老神经退行性疾病
《Cell》和《Nature》上的大量研究发现:NMN能有效延缓衰老引起的各种问题。哈佛医学院的研究发现NMN可以缓解衰老。
Therascience NMN产品是根据哈佛医学院教授方案提供200mg + 50 mg 白藜芦醇。
NMN进入体内变成NAD+后对能量和物质代谢产生重要作用。仅就三羧酸循环而言,三羧酸循环是人体三大营养(糖类、脂类、氨基酸)的*终代谢通路,也是糖类、脂类和氨基酸代谢联系的枢纽,三羧酸循环同时为有机体提供了大量能量是有机体能量枢纽。线粒体内的辅酶I(NAD)在TCA循环中接受电子传递还原成还原型辅酶I(NADH),1 mol辅酶I(NAD)可以生成3 mol ATP,是细胞生命活动能量的重要来源。
醌吡咯并喹啉作为人类营养中一种主要的氧化还原辅因子,PQQ与细胞中的蛋白相结合,并起到抗氧化剂的作用。PQQ以激活线粒体生物起源氧化代谢中的数个信号通路,刺激细胞生长与分化而著称。
众多国际性研究表明,PQQ对不同部位都起保护作用:人体细胞内的线粒体,有氧化性损伤的神经元,产生缺血性损伤的心肌可以和NADH+共同使用。
CELL-SSENTIEL®系列 Protect+. 细胞抗氧化+
高浓缩绿茶多酚、反式白藜芦醇 、硫辛酸 、硒 、锌、维生素B族、维生素C、天然维生素D3、天然维生素E
GH-nat术后恢复
人参皂苷、 L-精氨酸、L 赖氨酸、L-鸟氨酸α-酮戊二酸、L-瓜氨酸、支链氨基酸、钙、锌、维生素B族、维生素D3
促进血液循环,缩短康复时间,改善康复效果,防止肌肉萎缩,增强抵抗力
反式白藜芦醇
天然发酵98%提纯的反式白藜芦醇150.0 mg
天然维生素E 10.0 mg
虾青素
天然虾青素8.0mg、天然维生素E 1.8 mg
文献资料:
1.Nuo Sun, Richard J. Youle, Toren Finkel, Mitochondrial Theory of Aging and Other Aging Theories. Mol Cell. 2016 Mar 3; 61(5): 654–666衰老的线粒体基础
2.Birkmayer G. Nadh: The Energizing Coenzyme. McGraw Hill Professional, 1998 Nadh:增加活力的辅酶
3.Birkmayer. JGD. Coenzym-1 (NADH) – Eine wissenschaftlich bewiesene Anti-Aging-Substanz. Prevention and anti aging 2006: 340-348. 还原型辅酶I(NADH):经过科学证明的抗衰老物质
4.Nadlinger K, Westerthaler W, Storga-Tomic D, Birkmayer JGD. Extracellular metabolization of NADH by blood cells correlated with intracellular ATP levels. Biophys. Biochim Acta 2002; 1573: 177-182. 血细胞对NADH的细胞外代谢与细胞内ATP水平相关
5.Zhu K(1), Swanson RA, Ying W. NADH can enter into astrocytes and block poly(ADP-ribose) polymerase-1-mediated astrocyte death. Neuroreport. 2005 Aug 1;16(11):1209-12. NADH可以进入星形胶质细胞并阻断聚(ADP-核糖)聚合酶1介导的星形胶质细胞死亡
6.Demarin V, Podobnik-Sarkanji S, Storga-Tomic D, Kay G, Martinic-Popovic,M. Puretic B., Birkmayer JGD. ENADA/NADH improves cognitive impairment of Alzheimer patients. J. Tumor Marker Oncology 2003; 18:43-49. ENADA / NADH可改善阿尔茨海默氏症患者的认知障碍
7.Reibnegger G, Greilberger J, Juergens G. and Oettl K. The antioxidative capacity of ENADA®-NADH in humans. J. Tumor Marker Oncol. 2003; 18, 37-41. ENADA®-NADH在人体内的抗氧化能力
8.Lotfi R, Birkmayer J, Ghouni A, Metabolic and Anthropometric Effects of NADH RAPID Energy in Diabetic Type 2. Journal of Food Science and Engineering 6 (2016) 280-285. NADH RAPID能量在2型糖尿病患者中的代谢和人体测量作用
9.Birkmayer JGD, Vrecko C, Volc D, Birkmayer W.Nicotinamide adenine dinucleotide (NADH) – a new therapeutic approach to Parkinson’s disease: Comparison of oral and parenteral application. Acta Neurol Scand. 1993; 87: 32-35. 还原型烟酰胺腺嘌呤二核苷酸(NADH)-帕金森氏病的新治疗方法:口服和肠胃外应用的比较
10.Birkmayer JGD, Zhang JR, ed. Bagchi D, Preuss H. NADH in Cancer Prevention and Therapy. CRC Press 2005; chapter 33, 541- 554. NADH在癌症的预防和治疗中的应用
11.Grathwohl D, Klann M, Müller HM, Schlachter H, Berg A. Influence of NADH supplementation for the muscular energy supply in humans. Deutsche Zeitschrift für Sportmedizin, 11/2000. 补充NADH对人类肌肉能量供应的影响
12.Kay GG, Virre ES, Moline M. Stabilized NADH (ENADA) as Counter-Measure Jet Lag and Sleep Deprivation. J. Tumor Marker Oncol. 2001; 16 : 124-125. 稳定的NADH(ENADA)作为应对时差和睡眠不足的措施
13.陈永红, 杜冠华. 线粒体与衰老. 中国药理学通报 Chinese Pharmacological Bulletin 2000 Dec; 16( 5) : 485~