非酒精性脂肪肝病
脂肪超负荷肝病,通常被称为“苏打病”或“脂肪肝病”,在没有过量饮酒的情况下,现在是西方慢性肝病的主要原因。
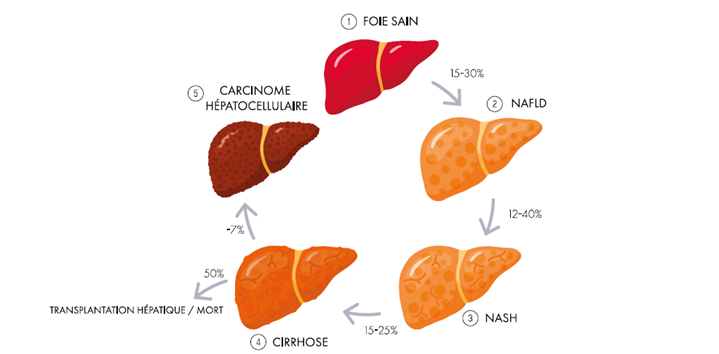
作为具有营养和环境成分的代谢疾病,这些病理范围从简单的非酒精性脂肪变性(NAFLD 或非酒精性脂肪肝病)到非酒精性脂肪性肝炎(NASH 或非酒精性脂肪肝炎),如果及时治疗是可以乔雅登。 酒精性脂肪性肝炎,可发展为纤维化和肝硬化、严重且不可逆的病症。
非酒精性脂肪肝病的特征是至少 5% 的肝细胞中甘油三酯异常积聚。它通常在没有明显临床症状的情况下发展。它与肥胖和代谢综合征密切相关,并且与心血管发病率和死亡率的增加独立相关。
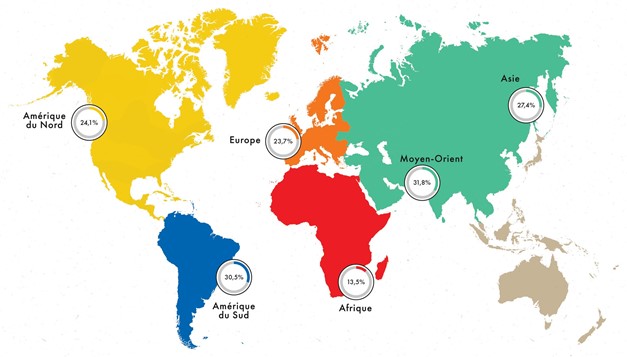
非酒精性脂肪肝病作为流行病影响所有国家。在法国,它影响了超过 20% 的人口,包括越来越多的青少年和年轻的超重受试者1-2。
在 12% 至 40% 的病例中,非酒精性脂肪肝病发展为非酒精性脂肪肝炎,这强调了实施早期筛查和管理的重要性。
由于迄今为止提出的各种药物治疗仅显示出有限的功效,因此生活方式和饮食措施的实施,包括使用适当的营养补充剂,至今仍是一种值得青睐的管理方法。
非酒精性脂肪肝病的发病机制很复杂,部分原因尚不完全清楚。
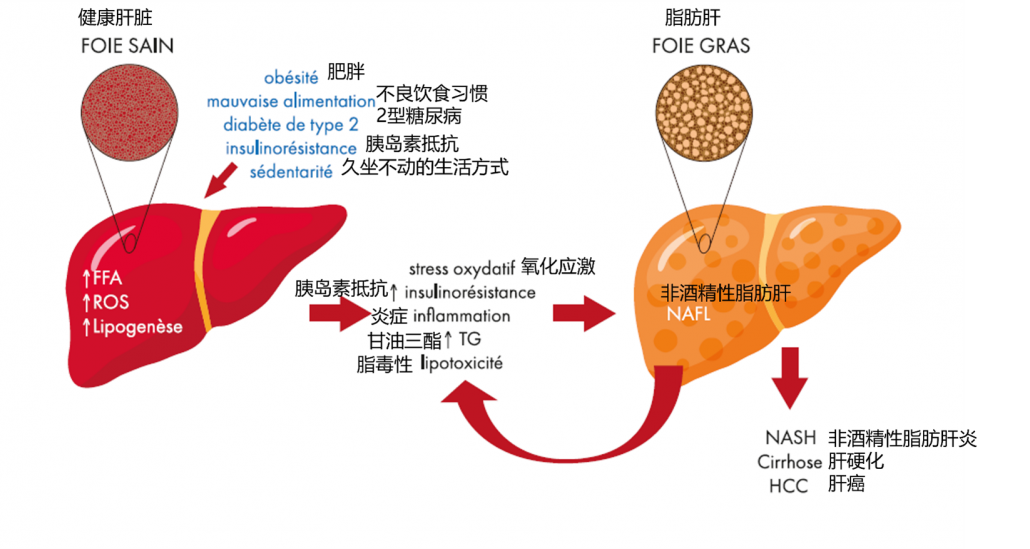
肥胖、胰岛素抵抗、高血压、高胆固醇血症和高甘油三酯血症等代谢综合征特征是非酒精性脂肪肝病发生的主要成分。事实上,肝脂肪变性和胰岛素抵抗之间的相互作用似乎是非酒精性脂肪肝病发展的两个关键因素,但很可能还有一个遗传因素导致非酒精性脂肪肝病的易感性与增加风险的遗传多态性有关。胰岛素抵抗和脂肪肝。
多因素机制导致非酒精性脂肪肝病中遇到的代谢功能障碍和生物参数紊乱。因此,报告了过度消耗食物和久坐的生活方式、果糖摄入、尿素循环紊乱、微生物群改变和线粒体功能障碍的作用。
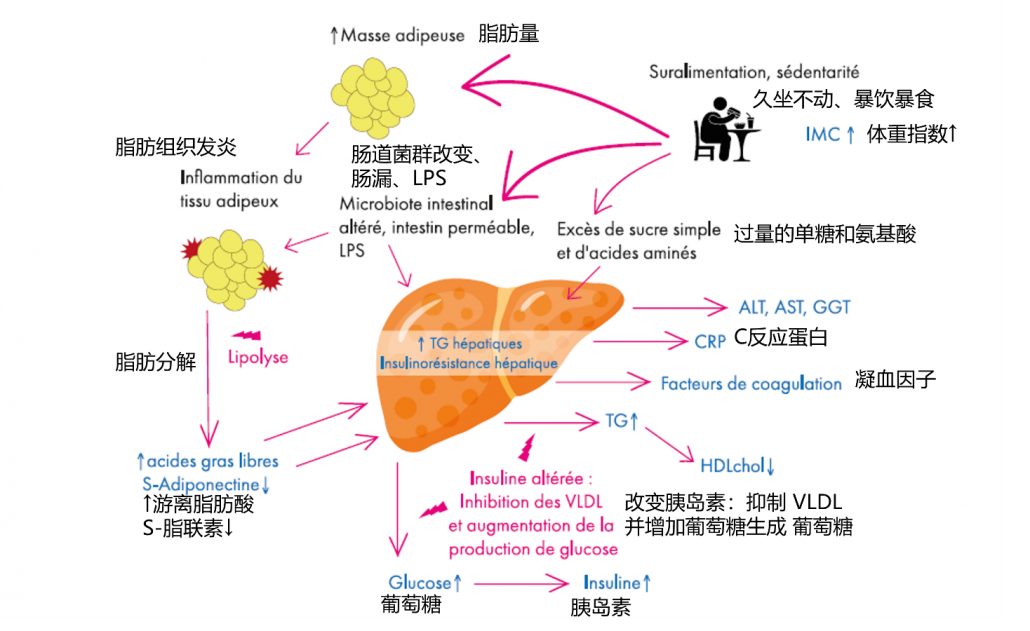
过度饮食和久坐不动的生活方式会导致脂肪组织扩张、缺氧和巨噬细胞浸润脂肪细胞。脂肪细胞的浸润诱导促炎细胞因子如 TNF- 和趋化因子如单核细胞趋化蛋白 1 的产生。这种炎症情况导致脂联素缺乏并促进游离脂肪酸的释放。
甘油三酯在肝脏中的积累是脂肪组织中游离脂肪酸流入的结果,也是它们合成增加的结果,以及原位甘油三酯输出的减少酸-氧化。
肝内脂质的积累会干扰细胞内胰岛素信号通路并维持肝胰岛素抵抗。
在所有情况下都存在胰岛素抵抗:
- 增加脂肪组织中甘油三酯的脂解作用,这是脂质过氧化的来源并增加促炎细胞因子的产生。
- 激活脂肪酸的重新合成,
- 增加肝内甘油三酯的储存,
- 减少极低密度脂蛋白的分泌和输出.
过量摄入果糖和添加糖:
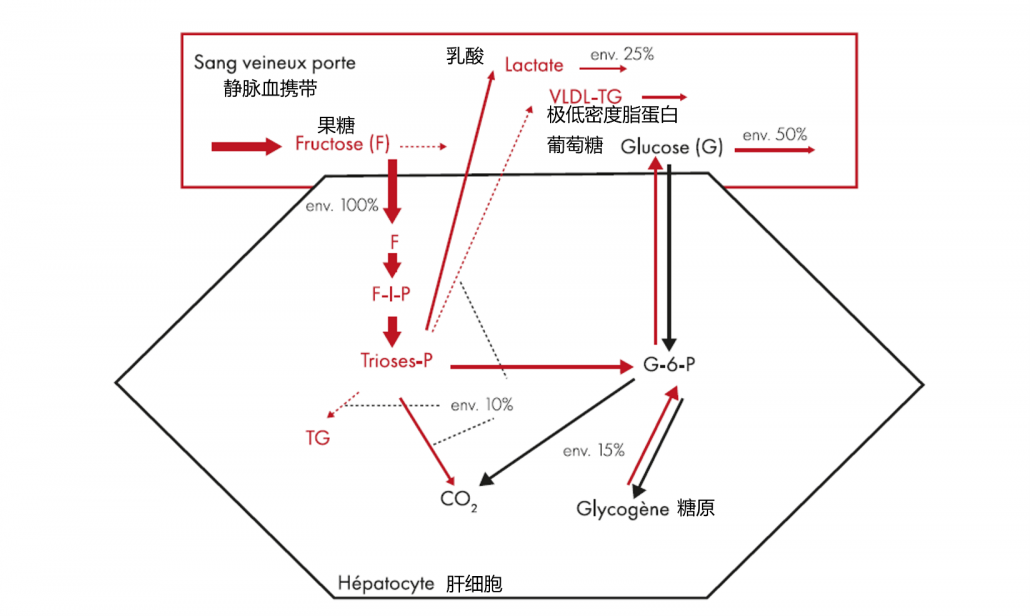
适度消耗(<50 g/d),果糖参与能量代谢和产热。 然而,过量时,它会诱导肝细胞的脂质超载。
在过去的几十年里,随着食品工业的发展,我们对果糖的消费量显着增加。 由玉米淀粉工业制备的高果糖糖浆存在于苏打水和许多工业食品中。 在西方饮食中,果糖和添加糖的摄入量估计超过 80 克/天,平均达到我们能量摄入量的 15%,对于青少年、年轻人和某些少数民族(太平洋岛屿、非洲美国人、南美洲人)
果糖的代谢不同于葡萄糖。 果糖的过量和长期消耗会导致肝细胞脂质超载,因为肝磷酸果糖激酶 C 对果糖的代谢会刺激脂肪酸的从头合成,阻止它们的氧化并降低能量消耗 。
同时,ATP的产生减少。 肝脏 ATP 产量的下降会引发一系列反应,包括氧化爆发、肠道通透性增加和线粒体功能障碍。
几种饮食因素会加剧非酒精性脂肪肝病的诱发:高脂肪、高盐、高血糖指数食物和酒精的饮食。
尿素循环中断和高氨血症:
肝脏是氨解毒的场所。 大多数氨基酸在肝脏中代谢,参与糖异生,或通过尿素循环和 NH4 产生排出体外。
在非酒精性脂肪肝病中,尿素循环酶的表达降低,导致肝毒性高氨血症。 因此,尿素循环和氨的调节是肝纤维化预防性治疗的目标。
微生物群改变:肠道通透性、细菌易位和肝脂肪变性之间的联系
通过肠通透性、细菌易位和肝脂肪变性之间的相关性,肠/肝轴与非酒精性脂肪肝病密切相关。 因此,在增加肠道通透性和肠道细菌易位的生态失调中,LPS 等化合物的产生及其通过门静脉向肝脏的迁移参与脂肪细胞和非酒精性脂肪肝病的肝脏炎症。
在微生物群的紊乱中,小肠最近被描述为与非酒精性脂肪肝病的密切相关。
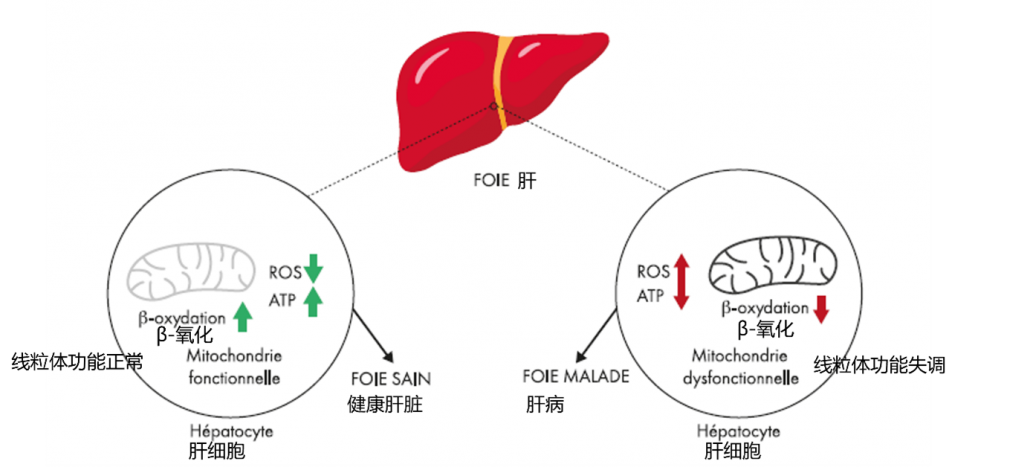
线粒体功能障碍
在 非酒精性脂肪肝病中,线粒体的生物发生和功能下降导致其氧化脂质的能力下降。 抑制-氧化和降低柠檬酸合酶 (CS) 活性会导致柠檬酸循环减慢、呼吸链复合物的活性降低和 ATP 的产生,以及产量的增加的激进物种。
生物自由基参数因此被修改,脂质和碳水化合物血浆分布失调。
通过生物活性化合物和微量营养素管理非酒精性脂肪肝病和非酒精性脂肪肝炎
与游离脂肪酸的流入和储存在肝脏中引发炎症氧化过程和线粒体毒性有关,这些具有强烈营养成分的疾病及其相关风险必须及早处理。
在没有证明其有效性的预防性药物治疗的情况下,治疗必须是:
- 通过卫生和饮食建议,这在任何治疗中都必不可少:减少热量摄入、减轻体重、反对久坐的生活方式、停止含有果糖的含糖饮料、坚持地中海饮食、定期进行体育锻炼等。
- 通过适当的补充:一些生物活性化合物和微量营养素已在临床上显示出它们对治疗非酒精性脂肪肝病的作用。
1. L-鸟氨酸-L-天冬氨酸盐(LOLA)
口服后,盐解离成 2 个组成氨基酸:L-鸟氨酸和 L-天冬氨酸,它们通过主动转运被吸收、分布和代谢,产生谷氨酰胺、谷胱甘肽和一氧化氮。
这些代谢物的产生解释了 L-鸟氨酸-L-天冬氨酸盐在慢性肝病中的保肝作用。
补充剂的保肝特性最近已在人体中得到临床证实,涉及:
- 谷胱甘肽的抗氧化和解毒特性,由鸟氨酸通过转氨作用生成谷氨酸。
- 通过增加从L-鸟氨酸、然后是L-精氨酸产生的一氧化氮来激活微循环。
- 谷氨酰胺的解毒作用增加了肝脏对尿素循环或谷氨酰胺合酶中过量NH4 的解毒能力。
LOLA补充剂的临床益处:
AST、ALT 非酒精性脂肪肝病组的效果比肝硬化组更明显,结果由第二项研究证实报告在补充 12 周后 ALT 和甘油三酯显着下降,并且通过断层扫描测量肝脏和脾脏显着改善 。
最后,在最近一项对 78 名非酒精性脂肪肝炎患者进行的试验,补充剂可改善肝脏微循环。
2. LA SILYMARINE 水飞蓟素
从水飞蓟 (Silybum marianum) 中提取的水飞蓟素是一组多酚类物质(水飞蓟宾 A 和 B、异西比林、水飞蓟素、水飞蓟素、异水飞蓟素和紫杉叶素)。 在所有这些化合物中,水飞蓟宾以最具生物活性的形式存在最多。
保肝特性和机制:
水飞蓟素通过抑制 Kupffer 细胞中 LT4 白三烯的形成而起作用,减轻炎症,并通过抑制纤维化诱导基因(如前胶原-和 TGF-)的表达,减少纤维化并刺激肝脏再生。
此外,它具有抗氧化和膜稳定活性,降低胰岛素抵抗并激活胆汁排泄。
补充的好处:
在 138 名非酒精性脂肪肝病患者中,摄入水飞蓟素(188 mg/d)12 个月,结合胆碱和维生素 E,使转氨酶正常化,减少 -GT,改善胰岛素抵抗和逆转脂肪变性。
在另一项与安慰剂比较的临床研究中,180 毫克/天的水飞蓟素 3 个月改善了非酒精性脂肪肝病患者患者的生物特征参数:腹围、BMI 和肝脏的组织学分析。 对 8 项研究和 587 名患者的荟萃分析证实了水飞蓟素对非酒精性脂肪肝病患者治疗效果。
3. 谷胱甘肽、乙酰谷胱甘肽和N-乙酰半胱氨酸
谷胱甘肽在调节自由基氧的产生和肝脏解毒中起着核心作用。 谷胱甘肽(L-谷氨酰-L-半胱氨酰甘氨酸)缺乏是肝细胞对氧化应激和细胞因子诱导的细胞死亡敏感性进展的主要因素之一。 在非酒精性脂肪肝病患者中观察到氧化爆发(增加 MDA、ox-LDL、TAC、SOD、GPx)和谷胱甘肽消耗。
口服谷胱甘肽通过刺激 PPArs-受体,增加脂肪酸的利用,降低血浆中游离脂肪酸、甘油三酯、铁蛋白和 ALAT的水平。
众所周知,补充谷胱甘肽或其前体 N-乙酰半胱氨酸对慢性肝病的益处。
S-乙酰谷胱甘肽 (S-GSH)
血液中 GSH 的寿命很短,这限制了其被细胞吸收。 通过使用具有更高稳定性和更好生物利用度的 S-乙酰谷胱甘肽 (S-GSH) 形式可以避免这一障碍,这种形式在被细胞吸收后直接转化为还原型谷胱甘肽。
N-乙酰半胱氨酸(NAC)
N-乙酰半胱氨酸是公认的谷胱甘肽前体,在 NAFLD 的管理策略中占有一席之地。 在人类中,NAC/二甲双胍组合可显着减少肝脂肪变性和纤维化。 最近的一项研究报告了补充NAC 3 个月(600 毫克/天)对 ALT 水平和脾脏大小的有效性 。
4. 熊果酸
熊果酸是一种五环三萜,具有抗炎和抗氧化、保肝和预防脂肪变性和代谢综合征的特性:调节脂肪生成、脂肪酸氧化、胰岛素抵抗、线粒体、糖异生、氧化应激和炎症。
熊果酸的几种作用机制:
- 碳水化合物稳态的调节:GLUT4 的易位和抑制淀粉酶和减少淀粉吸收,抑制果糖代谢。
- 降低甲基乙二醛的细胞毒性并刺激乙二醛酶系统。
- 减少脂肪细胞的分化
- 刺激线粒体脂肪酸氧化。
在动物模型中,熊果酸可减轻脂肪肝、纤维化和胰岛素抵抗
在人类中,熊果酸 150 毫克/天,持续 3 个月,可调节体重、胰岛素敏感性和血糖,并促进肝脏解毒 。
5. 非维生素 A 类胡萝卜素:番茄红素的好处
具有非维生素 A 原活性的类胡萝卜素在预防和治疗非酒精性脂肪肝病方面的潜力已被广泛报道,最近也有文献记载。
非酒精性脂肪肝病患者的血浆番茄红素水平较低,相反,高水平与非酒精性脂肪肝病的改善和 TG、HOMA-IR 和 BMI 降低有关。
最近证明,除了所有类胡萝卜素共有的抗氧化和抗炎作用外,摄入番茄红素对肝脂肪变性的益处还在于减少了编码脂肪生成基因(如 SREBP-1)的表达。
6. LA CHOLINE47-48胆碱47-48
胆碱是一种必需营养素,其代谢发生在肝脏中,其缺乏会伴随肝脏脂肪变性和肝细胞死亡。
胆碱的肝脏代谢通过磷脂酰胆碱形式,这是 极低密度脂蛋白中甘油三酯的输出和胆汁盐溶解所必需的。
在胆碱缺乏症中,观察到的肝脏疾病的起源有多种机制:甘油三酯合成异常、极密度脂蛋白分泌受损、线粒体功能障碍和氧化应激、肠道微生物群的干扰。
由于 极低密度脂蛋白输出的改变是脂肪变性的核心,胆碱需求的覆盖似乎对于预防脂肪变性至关重要。 在患有脂肪变性的受试者中,一项大型研究(>56,000 名患者)报告了 NAFLD 的出现与胆碱摄入量之间的反比关系。
总结
- 非酒精性脂肪肝病是一种日益流行的疾病,包括在儿童和青少年中。
- 任何患有代谢综合征、肥胖症、2 型糖尿病、肝功能检查异常或有心血管疾病病史的患者都应筛查非酒精性脂肪肝病。
- 生活方式和饮食措施以及生态失调的治疗构成了具体治疗的初步基础。
- 应尽早实施适当补充生物活性化合物,这些化合物已在发病机制的不同阶段显示出临床和生物学功效,目的是减少脂肪变性和使肝功能测试正常化。
文章来源 https://iepp-eu.com/wp-content/uploads/2013/04/IEPP-Lettre-n35-NASH-VDOC973-202009.pdf